پالادیوم آزمایشگاهی
- کم ترین چگال و کمترین نقطه ذوب فلزات گروه پلاتین
- ماده ای که مواد شیمیایی را تسریع می کند
- کاربرد های مهم پالادیوم در مبدل کاتالیزوری
پالادیوم یا پالادیم
پالادیوم یا پالادیم (Pd) یکی دیگر از محصولاتی است که در فروشگاه اینترنتی آریاطب عرضه می گردد
پالادیوم چیست
پالادیوم یا پالادیم Pd)) یک عنصر شیمیایی ، کم ترین چگال و کمترین نقطه ذوب فلزات گروه پلاتین در درجه 8-10 (VIIIb) و دوره های 5 و 6 جدول تناوبی می باشد، به ویژه به عنوان کاتالیزور ( ماده ای که مواد شیمیایی را تسریع می کند).مورد استفاده قرار میگیرد.
کاربرد پالادیوم
کاربرد های مهم پالادیوم در مبدل کاتالیزوری می باشد.
سطوح پالادیوم کاتالیزورهای عالی برای واکنش های شیمیایی شامل هیدروژن و اکسیژن مانند هیدروژناسیون ترکیبات آلی اشباع نشده هستند. در شرایط مناسب (80 درجه سانتی گراد [176 درجه فارنهایت] و 1 اتمسفر) ، پالادیوم بیش از 900 برابر حجم هیدروژن خود را جذب می کند. در این مرحله ، گسترش می یابد و سخت تر و انعطاف پذیرتر می شود. جذب پالادیوم همچنین هدایت الکتریکی و حساسیت مغناطیسی را کاهش می دهد. هیدرید یا آلیاژ فلزی تشکیل می شود که با افزایش دما و کاهش فشار می توان هیدروژن را از آن خارج کرد. زیرا هیدروژن در دمای بالا به سرعت از فلز عبور می کند. لوله های پالادیوم در برابر غشاهای نیمه تراوا در برابر سایر گازها نفوذ ناپذیر هستند و برای آوردن هیدروژن به داخل و خارج از سیستم های گاز بسته یا برای پردازش هیدروژن استفاده می شوند.
آزمایشگاهی پالادیوم
پالادیوم در حضور هوا سیاه نمی شود. این فلز با چگالی کم ، کمترین نقطه ذوب را در بین فلزات گروه پلاتین دارد. وقتی فلز گرم می شود ، به شدت کشیده و نرم می شود و در دمای بالا سفت می شود. پالادیوم به شدت با ترکیبات گوگرد و اسید نیتریک ترکیب می شود تا به آرامی در اسید کلریدریک حل شود. علاوه بر این ، این فلز در دمای معمولی با اکسیژن ترکیب نمی شود.
این فلز توانایی خیلی غیرعادی و عجیبی در جذب هیدروژن تا 900 برابر حجم خود در شرایط مناسب (دمای 80 درجه سانتیگراد و فشار 1 اتمسفر) دارد.
حالتهای اکسیداسیون معمولی پالادیوم +2 ، +3 و +4 است. اخیراً ، ترکیبات پالادیوم توسعه یافته اند که در آنها این عنصر دارای اکسیداسیون +6 هستند.
پالادیوم هم به عنوان فلز آزاد و هم به عنوان آلیاژی با طلا ، پلاتین و سایر فلزات در کوههای اورال استرالیا ، اتیوپی و آمریکای شمالی و جنوبی یافت می شود. با این حال ، بیشتر پالادیوم مصرفی به دلیل سودآوری از معادن نیکل و مس در آفریقای جنوبی و انتاریو به دست می آید ، زیرا حجم زیادی از این فعالیتها عملیات پالادیوم را استفاده می کند.
آزمایشگاهی پالادیوم چیست
پالادیوم یا پالادیوم یکی از عناصر شیمیایی جدول تناوبی می باشد. نماد کوتاه آن Pd و عدد اتمی آن 46 است و یکی از فلزات کمیاب است و نقره ای و سفید میباشد. پالادیوم فلزی از گروه پلاتین میباشد و کمترین چگالی و کمترین نقطه ذوب را در مقایسه با سایر فلزات این گروه دارد. این فلز کمیاب عمدتا از معادن مس و نیکل به دست می آید.
واکنش پالادیم
پالادیوم نسبت به سایر فلزات پلاتین واکنش پذیرتر می باشد. به عنوان مثال ، اسیدها راحت تر از سایر فلزات پلاتین مورد حمله واقع شوند. به آهستگی در اسید نیتریک حل می شود تا پالادیوم (II) نیترات ، Pd (NO3) 2 ، و با اسید سولفوریک غلیظ ، سولفات پالادیوم (II) ، PdSO4 2H2O تولید کند. در شکل اسفنجی ، حتی در اسید کلریدریک در حضور کلر یا اکسیژن حل می شود. به سرعت توسط اکسیدهای قلیایی و پراکسیدها و همچنین توسط فلورین و کلر در دمای 500 درجه سانتی گراد (932 درجه فارنهایت) ذوب می شود. هنگام گرم شدن ، پالادیوم با تعدادی عنصر غیر فلزی مانند فسفر ، آرسنیک ، آنتیموان ، سیلیسیم ، گوگرد و سلنیوم ترکیب می شود. مجموعه ای از ترکیبات پالادیوم را می توان با حالت اکسیداسیون +2 تهیه کرد. بسیاری از ترکیبات در حالت +4 و برخی در حالت 0 شناخته می شوند. در میان فلزات در حال انتقال ، پالادیوم یکی از قوی ترین گرایش ها برای اتصال به کربن را دارد. تمام ترکیبات پالادیوم به سانی تجزیه شده یا به فلز آزاد تبدیل میشوند.
واکنش پالادیوم بیشتر از سایر فلزات پلاتین می باشد. به عنوان مثال اسیدها به راحتی نسبت به سایر فلزات پلاتین مورد حمله قرار می گیرند. این ماده به آرامی در اسید نیتریک حل می شود و نیترات پالادیوم (II) ، Pd (NO3) 2 می دهد و با اسید سولفوریک غلیظ سولفات پالادیوم (II) ، PdSO4 2H2O تولید می کند. در شکل اسفنجی آن حتی در اسید کلریدریک در حضور کلر یا اکسیژن حل می شود. به سرعت توسط اکسیدهای قلیایی ذوب شده و پراکسیدها و همچنین توسط فلورین و کلر در دمای 500 درجه سانتیگراد (932 درجه فارنهایت) مورد حمله قرار می گیرد. پالادیوم همچنین با تعدادی از عناصر غیر فلزی در موقع گرم شدن مانند فسفر ، آرسنیک ، آنتیموان ، سیلیکون ، گوگرد و سلنیوم ترکیب می شود. یک سری از ترکیبات پالادیوم را می توان با حالت اکسیداسیون 2+ تهیه کرد. ترکیبات متعددی در حالت 4+ و تعداد کمی در حالت 0 نیز شناخته شده اند. در میان فلزات انتقالی پالادیوم یکی از قوی ترین تمایلات را برای ایجاد پیوند با کربن دارد. تمام ترکیبات پالادیوم به راحتی تجزیه شده و یا به فلز آزاد تبدیل می شوند.
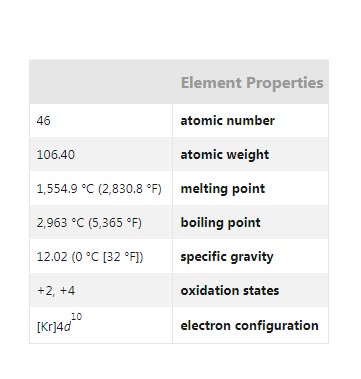
خصوصیات عنصر
پالادیوم از کجا بخرم
فروشگاه اینترنتی آریاطب یک شرکت فعال در زمینه فروش آنلاین مواد شیمیایی ، آزمایشگاهی و زیبایی است که آماده ارائه خدمات فروش مواد شیمیایی و زیبایی با کیفیت عالی ، قیمت مناسب ، کمیت و تعداد مورد نظر مشتریان عزیز می باشد.
آزمایشی پالادیوم
آدرس ایمیل شما منتشر نخواهد شد. فیلدهای الزامی علامت گذاری شده اند *

